Процесс каталитической конверсии уже полностью отработан. Для борьбы с отложением сажи а катализаторе при конверсии высокомолекулярных углеводородов к нему добавляется цемент. На заводах компании Стандард Ойл в Бейуэе и Батон-Руже метод каталитической конверсии используется значительное время. В качестве исходного сырья в Бейуэе используется газ нефтеперерабатывающего завода, в Батон-Руже природный газ. Так как никелевый катализатор отравляется серой, то газ необходимо очищать от сернистых соединений. [1]
Процесс каталитической конверсии в кипящем слое с применением инертного сепарирующегося теплоносителя должен пройти опробование в полупромышленных условиях. Он является перспективным в связи с возможностью увеличения мощности конверсионного агрегата и исключения большого числа жаропрочных труб. [2]
Процесс каталитической конверсии углеводородов осуществляется Е промышленности преимущественно в неподвижном слое катализатора. Поэтому кратко рассмотрим течение газа сквозь стационарный зернистый слой. [3]
Процесс каталитической конверсии углеводородов широко используется для получения не только водорода, но и азотоводородной смеси, применяемой в синтезе аммиака. Однако, несмотря на то, что между – этими производствами имеется много общего, ряд существенных различий не позволяет во всех случаях переносить опыт азотной промышленности для получения водорода. Так, при производстве водорода остаточное содержание метана после конверсии в печи не должно быть более 1 5 – 2 5 объемн. [5]
Обычно процесс каталитической конверсии осуществляется в трубчатых печах. В трубы, обогреваемые снаружи дымовыми газами, засыпан катализатор. [7]
Обычно процесс каталитической конверсии осуществляется в трубчатых печах. [8]
Схема процесса каталитической конверсии с водяным паром проста и состоит в следующем. Очищенный от сернистых соединений природный газ смешивают с водяным паром и пропускают над никелевым катализатором, помещаемым в вертикально расположенных трубах из легированной стали. [9]
В процессе окислительной каталитической конверсии происходит существенное увеличение содержания кислорода, особенно в смолистой части остатка 350 С – КК. Суммарный выход кислородсодержащих соединений с ростом температуры процесса уменьшается, что связано с их невысокой термической стабильностью и увеличением доли реакций полного окисления. [11]
В процессе каталитической конверсии углеводородов водяным паром также возможно выделение углерода. При 600 – 800 С образуется аморфная сажа, которая отлагается на поверхности и в порах катализатора. [13]
В процессе каталитической конверсии низкооктановых бензинов и лигроинов сырье прокачивается вначале через теплообменники, а затем через печь. Нефтяной продукт, подвергаемый превращению, нагревается до температуры 430 – 450; выходящие из печи пары поступают непосредственно в каталитическую камеру, а оттуда через теплообменники во фракционирующую колонну, где и разделяются на соответствующие фракции: авиационный бензин, лигроин и более тяжелые продукты. [14]
При совмещении процессов каталитической конверсии метана и оксида углерода при 2 0 МПа в одном агрегате газ после конвертора метана и увлажнителя при температуре 400 С и отношении пар: газ 1 187: 1 последовательно проходит конвертор 1 оксида углерода I ступени ( рис. И-39), испаритель 2 и конвертор 3 оксида углерода II ступени. В конверторах газ движется в радиальном направлении. Тепло газа, выходящего из конвертора СО, используют для нагревания исходной смеси природного газа и пара в теплообменнике. При этом температура конвертированной парогазовой смеси снижается с 430 до 310 С. Основное количество тепла конвертированной парогазовой смеси ( 80 %) используется в процессе очистки газа от диоксида углерода. Окончательное охлаждение газа с использованием его, тепла зависит от схемы производства и потребности в тепловой энергии. [15]
Http://www. ngpedia. ru/id341413p1.html
Аналогичная ситуация наблюдается и в нефтепереработке – на большинстве крупных НПЗ необходимость повышения глубины переработки при увеличении доли сырья с высоким содержанием серы ведет к существенному ужесточению режимов термокаталитических процессов, которое приводит к значительному росту содержания газообразных углеводородов С2-С4 (так называемые «жирные» газы, содержащие парафины и олефины). Зачастую этим «жирным» газам не удаётся найти рационального использования, и они также сжигаются на факелах. С другой стороны, превращение попутных и «жирных» газов, сжигаемых на факелах в местах нефтедобычи и на НПЗ, в жидкие углеводороды, являющиеся ценным сырьем для нефтехимической промышленности могло бы решить проблему их утилизации. Этим будет обеспечена как защита окружающей среды, так и экономия значительных количеств ценных природных ресурсов.
Перспективным направлением в вопросе прекращения сжигания попутных газов является квалифицированная каталитическая переработка и получение из них концентрата ароматических углеводородов, используемого как в нефтехимии (так называемая БТК-фракция – смесь бензола-толуола-ксилола), так и в нефтепереработке (высокооктановые компоненты автомобильных бензинов). ОАО «Новосибирский завод химконцентратов» в сотрудничестве с Институтом катализа СО РАН им. Г. К. Борескова, учеными которого разработана и промышленно апробирована каталитическая технология конверсии попутных газов, провел масштабную работу по освоению серийного производства катализаторов с использованием данной технологии.
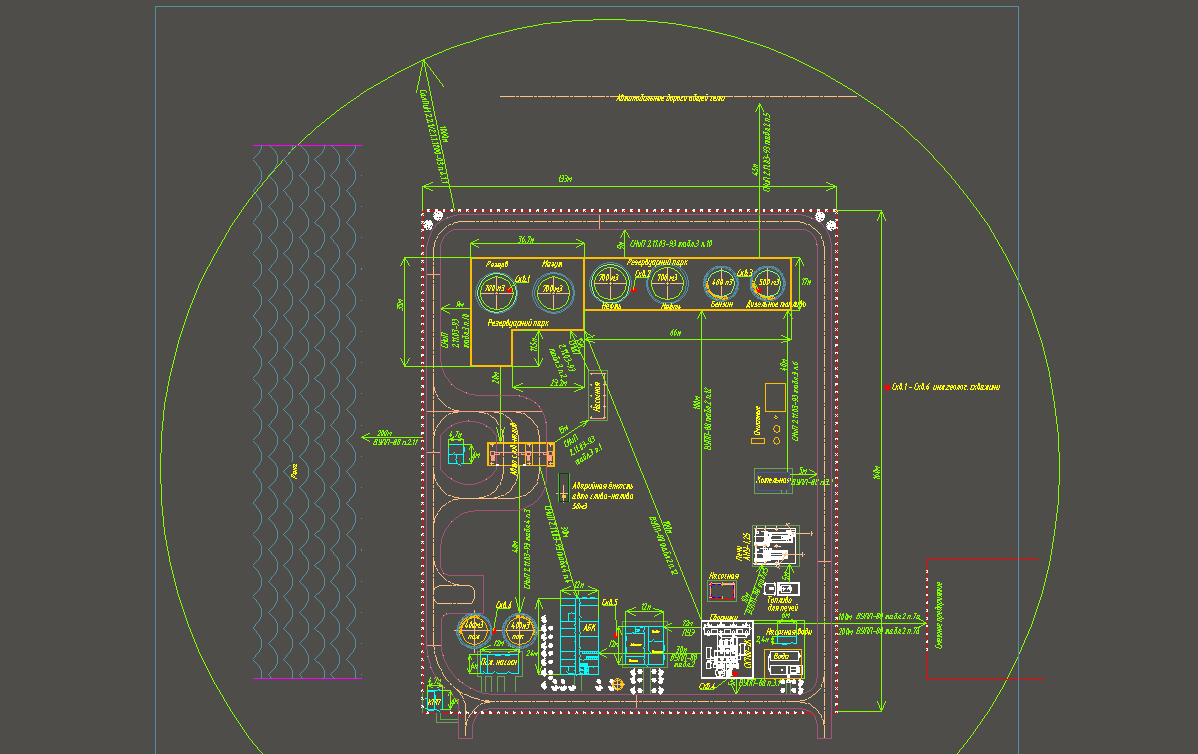
После очистки попутного газа от механических примесей и осушки от воды (см. рис. 1), он поступает в блок ароматизации, где его последовательно нагревают в рекуперационном теплообменнике и печи до температуры более 500оС, и при давлении до 10 атмосфер подают в каталитический реактор, заполненный неподвижным слоем катализатора. По мере прохождения слоя катализатора происходит конверсия легких парафиновых углеводородов С2-С4 в БТК-фракцию. После выхода продуктов из реактора образовавшиеся ароматические углеводороды отделяют в ректификационной колонне (блок разделения продуктов), а непрореагировавшие газовые компоненты возвращают на вход каталитического реактора. Периодически (с интервалом раз в 10-20 дней) проводят регенерацию катализатора путем его продувки азото-воздушной смесью. Цикл регенерации не превышает 80 – 100 часов. Для обеспечения непрерывной работы установки каталитический блок состоит из 3 реакторов, из которых два всегда находятся в режиме работы, третий в режиме регенерации.
Суммарный выход смеси ароматических углеводородов из прошедшего переработку попутного нефтяного газа может достигать 60 % (средние значения выхода без рециркуляции непрореагировавших газов – в диапазоне 30 – 35 %). Оставшаяся газообразная фракция (так называемый «сухой» газ) имеет параметры, близкие требованиям газотранспортной системы, и может направляться в газопровод для дальнейшей транспортировки.
Работоспособность основных технологических звеньев процесса (катализатор, каталитический реактор, система регенерации, система разделения продуктов) подтверждена в 2006 полномасштабными испытаниями в ОАО «НИПИгазпереработка» (г. Краснодар) на опытно-промышленной установке производительностью более 1,5 тыс. м3 газа/сутки на сырье, близком по составу к попутным нефтяным газам (см. рис. 2).
По итогам опытно-промышленных испытаний в ОАО «Ермак» (г. Новосибирск) разработан проект промышленного варианта установки. В разработанном варианте установка конверсии попутных нефтяных газов изготавливается в блочно-модульном исполнении, позволяющем транспортировку как на стандартных ж/д платформах, так и автотранспортом на трейлерах-длинномерах. Изготовитель также предусматривает оказание услуг по комплектации оборудованием и монтажу установки «под ключ».
После проведения в 2006 г. испытаний установки в ОАО «НИПИгазпереработка», комплекс работ по усовершенствованию технологии на ОАО «НЗХК» позволил заметно улучшить эксплуатационные свойства катализаторов (срок службы до 2-х лет, межрегенерационный пробег до 500 часов). В итоге технико-экономические показатели описанной технологии конверсии попутных газов значительно возросли. Сегодня существующая мощность производства на ОАО «НЗХК» составляет около 150 тонн/год, что уже сейчас позволяет комплектовать катализатором до 10-12 вышеописанных установок конверсии попутного газа.
Предлагаемая технология является на 100 % отечественной разработкой, при этом как по технологическому решению и составу оборудования, так и по показателям работы используемого катализатора не уступает зарубежным аналогам и превосходит их с точки зрения экономической целесообразности. Таким образом, сотрудничество ИК СО РАН и ОАО «НЗХК» демонстрирует пример позитивного взаимодействия сибирской науки и крупного промышленного производства в решении задач повышения глубины переработки нефтегазового сырья и минимизации экологического воздействия на окружающую среду, изложенных в одном из последний президентских посланий.
Http://www. ooomzm. ru/articles/47/
Химия и химические технологии/5. Фундаментальные проблемы создания новых материалов и технологий.
ПОЛУЧЕНИЕ ВОДОРОДА МЕТОДОМ ПАРОВОЙ КОНВЕРСИИ УГЛЕВОДОРОДНЫХ ГАЗОВ С УСОВЕРШЕНСТВОВАНИЕМ КОНСТРУКЦИИ НАГРЕВАТЕЛЬНОГО ЗМЕЕВИКА ПЕЧИ КОНВЕРСИИ
Основной путь развития нефтепереработки связан с ростом потребления водорода. Он включает развитие процессов гидрооблагораживания нефтепродуктов и гидрокрекинга для получения моторных горючих и малосернистого котельного горючего. Весь автобензин должен иметь октановое число от 90 до 93 по исследовательскому методу и содержание серы не более 0,05-0,10 % (масс.). Содержание серы в дизельном топливе не должно превышать 0,2 % (масс.) [2].
Таким образом, нефтеперерабатывающая и нефтехимическая промышленность становится крупным потребителем водорода. Поэтому на заводах перерабатывающих сернистые и высокосернистые нефти должны быть сооружены мощные установки получения водорода [1].
В настоящее время основным методом производства водорода на нефтеперерабатывающих заводах является паровая каталитическая конверсия углеводородных газов в трубчатых печах.
Водород получают паровой конверсией углеводородов и очищают короткоцикловой адсорбцией. Доминирующие виды сырья для процессов паровой конверсии – природный газ, сжиженный нефтяной газ.
Углеводородное сырье подогревают и пропускают через аппарат гидроочистки, в котором непредельные соединения насыщаются. После этого сырье поступает в аппараты сероочистки, в которых адсорбируется сероводород.
Очищенное сырье смешивают с паром и перегревают в печном змеевике. Затем смесь пропускают через печные трубы, заполненные никелевым катализатором, на котором углеводороды реагируют с паром, при этом образуется смесь водорода и оксидов углерода с высоким содержанием водорода:
Реакция протекает при температуре от 800 до 900 0 С и давлении от 1 до 2,5 МПа [3].
Паровая конверсия углеводородного газа водяным паром с целью получения водородсодержащего газа осуществляется в многорядной трубчатой печи, которая состоит из топочной (радиантной) камеры и блока использования тепла дымовых газов (конвективной камеры) со встроенным вспомогательным котлом. В радиантной камере размещены реакционные трубы, образующие трубные экраны. Трубы заполнены катализатором и соединены с коллекторами входа парогазовой смеси и выхода конвертированного газа. Для обеспечения протекания эндотермической реакции конверсии метана сжигают топливный газ, подаваемый в панельные горелки. Теплота эндотермической реакции конверсии передается от продуктов сгорания в печи, температуру которой тщательно регулируют.
Конвертированный газ охлаждают в котле-утилизаторе, где вырабатывается технологический пар, после чего подают в конверторы СО. Здесь в слое железохромового катализатора, промотированного медью, СО реагирует с паром, давая водород и СО2.
После конверторов СО конвертированный газ охлаждается в подогревателях сырья, питательной воды и блока деаэрации питательной воды. Горячий конденсат отделяют от конвертированного газ, после чего газ охлаждают в воздухоподогревателе и холодильнике. Охлажденная смесь поступает в сепаратор конденсата, из которого газ идет в систему короткоцикловой адсорбции, где водород очищают от метана и оксидов углерода.
Система очистки работает в циклическом режиме – повторяются две основные стадии (адсорбции и регенерации). Очищенный водород выделяется под давлением, практически совпадающим с давлением сырья, а примеси – при более низком давлении. Адсорбент регенерируют снижением давления и продувкой. Адсорбент регенерируют снижением давления и продувкой. Отходящий газ из этой системы идет в горелки печи конверсии, за счет чего обеспечивается основная часть потребностей в тепле. Водород после очистки выводится за пределы установки. Термический КПД оптимизируют, рекуперируя теплоту дымовых газов печи конверсии и конвертированного газа. За счет этой теплоты подогревают сырье и вырабатывают пар на собственные нужды и на продажу. Из конвективной камеры дымовые газы дымососом выбрасываются в трубу.
Процессы паровой конверсии могут дать определенные преимущества потребителям водорода в небольших объемах. Так метод паровой конверсии углеводородных газов технологически и аппаратурно хорошо разработан и является экономически наиболее эффективным. Данный метод позволяет получать водород чистоты 99,9 % [4].
В настоящее время паровая каталитическая конверсия углеводородных газов в трубчатых печах является основным методом производства водорода на нефтеперерабатывающих и нефтехимических заводах. Это объясняется тем, что данный метод обладает рядом таких преимуществ, как: получение водородсодержащего газа с более высоким содержанием водорода; более низкие эксплуатационные затраты по сравнению с другими методами; использование в качестве сырья заводских газов; обеспечение установки паром собственной выработки. Также метод технологически и аппаратурно хорошо разработан и является пока экономически наиболее эффективным.
В результате проведенного нами патентного поиска был найден способ повышения эффективности работы установки получения водорода. Этого можно достигнуть с помощью изменения конструкции нагревательного змеевика трубчатой печи. Данное новшество позволяет снизить гидравлическое сопротивление в реакционных трубах и повысить выход целевого продукта.
Способ получения водородсодержащего газа в трубчатой печи с отношением длины реакционной трубы к ее диаметру, равным от 50 до 150, путем каталитической конверсии природного газа в присутствии пара при повышенных температуре и давлении. Способ отличается тем, что, с целью снижения гидравлического сопротивления и повышения выхода целевого продукта за счет увеличения времени контакта, конверсию осуществляют последовательно в двух зонах реакционной трубы. При этом парогазовую смесь подают в первую зону со скоростью от 1 до 35 м/с, а во вторую зону со скоростью от 0,01 до 0,30 м/с и температуру в первой зоне поднимают от 450 о С до 700 о С, а во второй зоне до от 830 до 860 о С способу получения водородсодержащего газа, в котором конверсию осуществляют в двух зонах реакционной трубы. Разделение реакционного пространства на две зоны целесообразно тем, что в первой зоне при большой скорости потока (от 1 до 35 м/с) возможно быстро подогреть исходную парогазовую смесь до температуры интенсивного протекания реакции во второй зоне.
В результате выполненного технологического расчета было установлено, что предложенное новшество позволяет повысить выход чистого водорода на 0,07 % объемных. Таким образом, повышение выхода целевого продукта дает возможность получить дополнительный доход и повысить рентабельность производства.
1. М. К.Письмен. Производство водорода в нефтеперерабатывающей промышленности. М.: Химия, 1980 г.
2. Справочник. Водород, свойства, получение, хранение, транспортирование, применение. М.: Химия, 1989г.
Http://www. rusnauka. com/20_AND_2014/Chimia/5_174313.doc. htm
Использование: в способах каталитической конверсии природного газа. Сущность изобретения: природный газ взаимодействует на никелевом катализаторе с парогазовой смесью, содержащей водяной пар и углекислый газ, при объемном соотношении природный газ : парогазовая смесь, равном 1:25-30, и давлении 1-4 атм. Взаимодействие проводят при 700-800 o C. 1 з. п. ф-лы.
Изобретение относится к области химической технологии, конкретно к способам каталитической конверсии природного газа и может быть использовано в технологических комплексах, в которых наряду с процессом конверсии природного газа и последующим производством из него метанола, технического водорода или аммиака вырабатывает электроэнергию.
Известен способ двухступенчатой каталитической конверсии природного газа (преимущественно метана) в синтез-газ (смесь водорода и оксида углерода), который служит исходным сырьем для крупнотоннажных производств метанола, технического водорода и аммиака. Первую стадию проводят в трубчатой печи с огневым обогревом реакционных труб, так что температура их теплообменной поверхности достигает 900-950 o C, при этом перепад давления составляет от 40-60 атм и выше в реакционных трубах до 1-2 атм в межтрубном пространстве. Вторую стадию проводят в шахтном реакторе, в котором необходимую для окончания процесса конверсии теплоту получают путем частичного сжигания смеси, поступающей с первой ступени [1] Осуществление первой стадии конверсии природного газа в трубчатой печи с множеством горелочных устройств характеризует способ в целом высоким удельным расходом природного газа, низкой эксплуатационной надежностью и как загрязняющий окружающую среду продуктами сгорания.
Наиболее близким по технической сущности и достигаемому результату изобретения является способ, в котором первую стадию конверсии природного газа проводят в реакторе-теплообменнике, вторую в шахтном реакторе. На первой стадии в реакционные трубы реактора-теплообменника подают смесь природного газа и водяного пара в соотношении от 1:2 до 1:4, где при 600-800 o C происходит разложение большей части метана. На второй стадии процесса частично конвертированный газ подают в шахтный реактор, где в пустом пространстве над катализатором его смешивают с кислородом или воздухом в соотношении кислород:углерод равном 0,4-0,45. При выгорании кислорода температура реакционной смеси повышается до 1400-1500 o C, которую затем направляют на слой никелевого катализатора, где за счет физического тепла конвертированного газа, происходит процесс доконверсии остаточного метана. Газовый поток, покидающий шахтный реактор, с температурой 900-1200 o C подают в межтрубное пространство реактора-теплообменника, где за счет тепла продуктов реакции второй ступени в реакционных трубах происходит первичный процесс конверсии метана. Обе стадии ведут при одинаковом давлении, которое может варьироваться от 20 до 300 атм [2] Однако организация теплообмена между интенсивными технологическими потоками ведет к созданию устройств, обладающих большой массой и значительными габаритами, в которых неизбежно возникает тепловые потери, связанные с наличием высоких градиентов температур между горячими и холодными потоками. Совместное действие высоких давлений и температур, при которых ведут процесс, приводит к необходимости применения высококачественных конструкционных материалов. Сжигание части продуктов конверсии первой ступени, вызывает дополнительный расход природного газа.
Задача изобретения создание способа каталитической конверсии природного газа, в котором устраняются эти недостатки.
Задачу в предлагаемом способе решают тем, что взаимодействие природного газа проводят при давлении 1 4 атм со смесью водяного пара с углекислым газом при соотношении природный газ парогазовая смесь равном 1 25 30. Предпочтительно взаимодействие проводить при 700 800 o C.
Существо предлагаемого способа состоит в том, что природный газ смешивают при давлении 1 4 атм в объемном соотношении 1:25-30 с парогазовой смесью, имеющей температуру порядка 700-800 o C и состоящей из водяного пара и углекислого газа. Полученную таким образом реакционную смесь направляют в реактор шахтного типа с загруженным никелевым катализатором, где за счет физического охлаждения исходной смеси проводится одностадийный процесс паро-углекислотной конверсии метана в синтез-газ. Исходную парогазовую смесь с указанными характеристиками получают с выхлопа турбины газотурбинной энергетической установки, в которой окислителем углеводородного топлива служит кислород. В качестве топлива может быть использована часть продуктов конверсии метана, непревращенных в метанол или оставшихся после выделения водорода.
Пример 1. Природный газ, очищенный от сернистых соединений, состоящий на 97% из метана и парогазовую смесь, полученную с выхлопа турбины газотурбинной установки, в которой окислителем углеводородного топлива служит кислород, в соотношении 1:28 подают в смеситель. Парогазовая смесь состоит на 63% из водяного пара и на 37% из углекислого газа. Газовые потоки смешиваются при температуре 720 o C и давлении 3 атм, в результате образуется газообразная смесь следующего состава об.
CH4 3,5 H2O 60,8 CO2 35,7 которую подают в шахтный реактор с никелевым катализатором. При каталитическом взаимодействии метана с водяным паром и углекислым газом, сопровождающимся охлаждением реакционной смеси, образуется синтез-газ. Синтез-газа на выходе из реактора имеет температуру равную 568 o C и следующий состав об.
Степень конверсии метана в этих условиях составляет 93% После конденсации воды полученный газ может быть использован для синтеза метанола.
Пример 2. Процесс проводят аналогично примеру 1 при давлении p 4 атм, температуре газа на выходе в реактор 800 o C, соотношении метан: парогозовая смесь равным 1 25.
В этих условиях синтез-газа на выходе из реактора имеет температуру равную 627 o C и следующий состав об.
Пример 3. Процесс проводят аналогично примеру 1 при давлении p 1 атм, температуре газа на входе в реактор 700 o C, соотношении метана парогазовая смесь равным 1 30.
В этих условиях синтез-газа на выходе из реактора имеет температуру равную 556 o C и следующий состав об.
Таким образом предлагаемый способ позволяет проводить конверсию природного газа в одну стадию без внешнего теплообмена, что приводит к сокращению удельного расхода природного газа на 20% и улучшению массо-габаритных характеристик установки, реализующей этот процесс.
1. Способ каталитической конверсии природного газа, включающий взаимодействие на никелевом катализаторе природного газа с реагентом, содержащим водяной пар, отличающийся тем, что в качестве реагента, содержащего водяной пар, используют парогазовую смесь, содержащую водяной пар и углекислый газ, взаимодействие природного газа с парогазовой смесью ведут при объемном соотношении природный газ: парогазовая смесь, равном 1 25 30, и давлении 1 4 атм.
2. Способ по п.1, отличающийся тем, что взаимодействие природного газа с парогазовой смесью ведут при 700 800 o С.
Http://www. findpatent. ru/patent/209/2097314.html
Катализ – это одна из наиболее динамично и стремительно развивающихся областей науки и техники. Непрерывно разрабатываются новые и совершенствуются существующие каталитические системы, предлагаются новые каталитические процессы, меняется их аппаратурное оформление, совершенствуются и появляются новые физико-химические методы исследования катализаторов. Большинство химических процессов, задействованных на предприятиях нефтехимического и нефтеперерабатывающего комплекса, являются каталитическими. Развитие катализа и каталитических технологий в значительной мере обуславливают конкурентную способность нефтехимической продукции на рынке. Поэтому остро стоит вопрос о необходимости подготовки высококвалифицированных специалистов в области катализа для нефтехимии.
Катализ – явление специфичное. Нет веществ, которые обладали бы каталитическими свойствами в общей форме. Для каждой реакции должен использоваться свой особый катализатор.
Применение катализа в химической промышленности. Каталитические процессы используются для получения водорода, служащего сырьем для синтеза аммиака и ряда других производств химической технологии. Конверсия метана. Наиболее дешевым источником водорода является природный газ. Первая стадия получения водорода включает взаимодействие метана с водяным паром при частичном добавлении кислорода или воздуха при температуре 800 – 1000°С (реакция 2.1). В качестве катализатора используется никель, нанесенный на термостойкие алюмооксидные носители (корунд – a-Al2O3).
В результате этой реакции наряду с водородом в значительном количестве образуется оксид углерода.
Конверсия СО. Взаимодействие оксида углерода с водяным паром осуществляют в две стадии при снижающемся температурном режиме с использованием оксидных катализаторов (реакция 2.2), при этом дополнительно образуется водород. На первой стадии применялся среднетемпературный (435-475°С) железохромовый катализатор (Fe3O4 с добавками Cr2O3); на второй – низкотемпературный (230-280°С) катализатор (смесь оксидов алюминия, меди, хрома и цинка). Конечное содержание оксида углерода, присутствие которого резко уменьшает активность железного катализаторов синтеза аммиака, может быть снижено до десятых долей процента.
Для удаления остатков СО необходимо было применять сложную промывку газовой смеси аммиачным раствором Сu2О под высоким давлением 120-320 атм и низкой температуре 5-20°С.
В практике промышленного производства очистку газовых выбросов от СО проводят методом абсорбции растворами Cu-аммиачных солей (формиатами и карбонатами меди), которые обладают способностью образовывать с СО комплексные соединения. Так как формиаты мало устойчивы, то предпочтение отдают карбонатным растворам.
Исходный карбонатно-аммиачный комплекс меди имеет следующий состав (кмоль/м 3 ): Cu + – 1,0 – 1,4; Cu 2+ – 0,08 – 0,12; NH3 – 4,0 – 6,0; СО2 – 2,4 – 2,6.
Абсорбционной способностью по отношению к СО обладают соли одновалентной меди. Катионы Cu 2+ участия в абсорбции, как правило, не принимают. Однако в растворе необходимо поддерживать концентрацию Cu 2+ не менее 10 мас. % от содержания Cu + . Последнее позволяет предотвратить образование осадка элементарной меди, которая может забить трубопроводы и нарушить работу абсорбера. Наличие в растворе карбонатно-аммиачного комплекса меди Cu 2+ смещает равновесие реакции (1) в сторону образования Cu + : Cu 2+ + Cu ⇄ 2 Cu + (1)
Процесс абсорбции СО карбонатно-аммиачным комплексом меди протекает по реакции: [Cu(NH3)2] + + CO + NH3 ⇄ [Cu(NH3)3CO] + – DH (2)
Метанирование. В связи с разработкой нового активного никелевого катализатора сложная операция отмывки может быть заменена при 250-350°С более простым процессом превращения остатка оксида углерода в инертный для катализатора синтеза аммиака метан (реакция 2.3):
Таким образом, разработка более активного катализатора позволила существенно упростить технологическую схему и повысить эффективность производства аммиака.
Применение катализа в нефтеперерабатывающей промышленности. Эффективность применения катализа оказалась столь значительной, что за несколько лет в нефтеперерабатывающей промышленности произошла подлинная техническая революция, позволившая на основе применения катализаторов резко повысить как выход, так и качество получаемых моторных топлив.
В настоящее время свыше 80% нефти перерабатывается с использованием каталитического процессов: крекинга, риформинга, изомеризации и гидрирования углеводородов, гидроочистки нефтяных фракций от серосодержащих соединений, гидрокрекинга. В таблице 2.1 приведены важнейшие современные каталитические процессы нефтепереработки.
Крекинг. Каталитический крекинг нефти или ее фракций является деструктивным процессом, осуществляемый при температурах 490-540°С на синтетических и природных алюмосиликатных катализаторах кислотной природы, для получения высококачественного бензина с октановым числом 98-92, значительного количества газов, содержащих предельные и непредельные углеведороды С3-С4, керосино-газойлевых фракций, технического углерода и кокса.
Октановое число (О. ч.) – условный показатель детонационной стойкости легких (бензинов, керосинов) моторных топлив при сгорании в карбюраторных двигателях. Эталонное топливо – изооктан (О. ч. = 100), нормальный гептан (О. ч. =0). Октановое число бензина – это процентное (по объему) содержание изооктана в такой его смеси с н-гептаном, которая при стандартных условиях испытания на специальном одноцилиндровом двигателе детонирует также, как испытуемый бензин.
В последние годы широкое промышленное использование получили катализаторы на основе кристаллических синтетических цеолитов. Активность этих катализаторов, особенно содержащих смесь оксидов редкоземельных элементов (СеО2, La2O3, Ho2O3, Dy2O3 и других), значительно выше, чем аморфных алюмосиликатных катализаторов.
Применение катализаторов позволило не только увеличить в 500-4000 раз скорость образования углеводородов более низкой молекулярной массы из нафтенов, но и повысить выход ценных фракций по сравнению с термическим крекингом.
Каталитический крекинг является наиболее высокотоннажным промышленным каталитическим процессом. С его помощью в настоящее время перерабатывается свыше 300 млн. т нефти в год, что требует ежегодного расхода около 300 тыс. т катализаторов.
Риформинг. Каталитический риформинг осуществляют при температуре 470-520°С и давлении 0,8-1,5 МПа на Pt, Re – катализаторах, нанесенных на оксид алюминия, обработанный хлористым водородом для увеличения кислотных свойств. Риформингом называют способ переработки нефтепродуктов, преимущественно, бензиновых и лигроиновых фракций нефти (углеводороды С6-С9 трех основных классов: парафиновые, нафтеновые и ароматические) с целью получения высокооктановых автомобильных бензинов, ароматических углеводородов (бензола, толуола, ксилола, этилбензола) и технического водорода. В процессе риформинга протекают реакции дегидрирования нафтенов в ароматические углеводороды, циклизации парафинов и олефинов и изомеризации пятичленных циклических углеводородов в шестичленные. В настоящее время каталитический риформинг используется для переработки более 200 млн. т нефти в год. Его применение позволило не только повысить качество моторного топлива, но и вырабатывать значительные количества ароматических углеводородов для химической промышленности. Побочными продуктами каталитического риформинга являются топливный газ, состоящий в основном из метана и этана, а также сжиженный газ – пропан-бутановая фракция
Гидроочистка нефтепродуктов. Ценным побочным продуктом каталитического риформинга является водород. Появление дешевого водорода позволило широко использовать каталитическую гидроочистку нефтепродуктов от серо-, азото – и кислородсодержащих соединений, с образованием легко удаляемых Н2S, NH3 и H2O, соответственно (реакции 2.4 – 2.7):
Одновременно происходит гидрирование диенов, что повышает стабильность продукта. Для этой цели наибольшее распространение получили катализаторы, приготовляемые из оксидов кобальта (2–5 масс.%) и молибдена (10-19 масс.%) или оксидов никеля и молибдена, нанесенные на γ-оксид алюминия.
Гидроочистка позволяет получать до 250-300 тысяч тонн элементарной серы в год. Для этого реализуют процесс Клауса:
Часть H2S окисляется кислородом воздуха на γ-Al2O3 при 200-250°С (реакция 2.8); другая часть H2S взаимодействует с диоксидом серы с образованием серы (реакция 2.9).
Условия проведения гидроочистки зависят от свойств очищаемого сырья, но чаще всего лежат в пределах 330-410°С и 3-5 МПа. Гидроочистке подвергается ежегодно около 300 млн. т нефтепродуктов (бензиновые и керосиновые фракции, дизельное топливо, вакуумные дистилляты, парафины и масла). Реализация в нефтепереработке стадии гидроочистки позволила подготовить сырье для каталитического риформинга (бензины) и крекинга (вакуумные дистилляты), получить малосернистые осветительный керосин и топливо, повысить качество продуктов (парафины и масла), а также имеет значительный экологический эффект, так как снижается загрязнение атмосферы выхлопными газами при сжигании моторного топлива. Внедрение гидроочистки позволило использовать высокосернистые нефти для получения нефтепродуктов.
Гидрокрекинг. В последнее время значительное развитие получил процесс гидрокрекинга, при котором одновременно осуществляются реакции крекинга, изомеризации и гидроочистки. Гидрокрекинг – это каталитический процесс глубокого превращения сырья различного фракционного состава в присутствии водорода с целью получения светлых нефтепродуктов: бензина, реактивного и дизельного топлива, сжиженных газов С3-С4. Применение полифункциональных катализаторов позволяет осуществлять этот процесс при 400-450°С, давлении около 5-15 МПа. В качестве катализаторов используют сульфид вольфрама, смешанные вольфрам-никелевые сульфидные катализаторы на носителях, кобальт-молибденовые катализаторы на оксиде алюминия, с добавками Ni, Pt, Pd и других металлов на аморфных или кристаллических цеолитах.
Таблица 2.1 – Современные каталитические процессы нефтепереработки
Http://helpiks. org/6-51773.html
Первые органические вещества, с которыми познакомился человек, были выделены из растительных и животных организмов или из продуктов их жизнедеятельности. Каждый растительный или животный организм представляет собой своеобразную химическую лабораторию в которой протекает множество сложнейших реакций, приводящих к образованию огромного числа органических веществ, как весьма простых (например, метан, муравьиная, щавелевая кислоты и т. п.), так и самых сложных (например, алкалоиды, стероиды, белки).
Характерной чертой органического синтеза у растений является накопление потенциальной химической энергии путем превращения в нее энергии солнечных лучей. С помощью хлорофилла на свету растения синтезируют сложнейшие органические соединения из самых простых химических веществ, в конечном счете, из двуокиси углерода, улавливаемой из воздуха, из воды и из минеральных солей, находящихся в почве. По всей вероятности, первичными продуктами фотосинтеза являются углеводы, которые в дальнейшем превращаются в жиры и белковые вещества растительных организмов. Фотосинтез у растений сопровождается выделением кислорода, который, как теперь точно установлено, образуется не из двуокиси углерода, а из воды. Таким образом, путем фотосинтеза в растениях происходит накопление сложных органических веществ. Естественно, что растения в большей мере, чем животные, служат первоисточником получения органических веществ.
Особенно богатым источником органических веществ являются древесные растения.
Наиболее давно известны термические методы переработки древесины, приводящие к разрушению содержащихся в ней сложных органических веществ с образованием более простых соединений.
Химическое производство основано на использовании в качестве сырья доступных, относительно дешевых, широко распространенных или возобновляющихся материалов. Наиболее важными природными источниками углеводородов являются природный и попутный нефтяной газы, нефть и каменный уголь. Особое внимание в последнее время также уделяется использованию отходов сельскохозяйственного производства, вторичной переработке промышленных и бытовых отходов.
Запасы природного газа на нашей планете велики. Природный газ представляет собой смесь газов, состав которой в значительной мере определяется месторождением. Однако в любом случае основным компонентом является метан, объемная доля которого колеблется от 70 до 98%. Остальные компоненты – это этан, пропан, бутан, изобутан, неорганические газы (азот, углекислый и благородный газы). Чем больше относительная молекулярная масса углеводорода, тем меньше его содержание в природном газе.
Попутный нефтяной газ растворен в нефти или находится над ней, образуя своеобразную «газовую шапку». В процессе добычи нефти его отделяют и используют в качестве топлива или химического сырья. В попутном газе содержится значительно меньше метана и больше его гомологов, чем в природном газе.
Для практических целей попутный газ разделяют на фракции: газовый бензин (смесь пентана, гексана и других алканов), пропан-бутановая фракция (смесь пропана и бутана) и сухой газ (сходен по составу с природным).
В органическом синтезе применяют как чистый оксид углерода, так и его смеси с водородом (синтез – газ) в объемном отношении от 1:1 до 2 – 2,3:1. Оксид углерода СО представляет собой бесцветный трудно сжижаемый газ ( температура конденсации при атмосферном давлении – 1920С, критическое давление 3,43 МПа, критическая температура – 1300С). С воздухом образует взрывоопасные смеси в пределах концентраций 12,5 – 74 % (об.). Оксид углерода является весьма токсичным веществом, его предельно допустимая концентрация (ПДК) в производственных помещениях составляет 20 мг/м3. Обычные противогазы его не адсорбируют, поэтому применяют противогазы изолирующего типа или имеющие специальный гопкалитовый патрон, в котором находятся оксиды марганца, катализирующие окисление СО и СО2. Оксид углерода слабо сорбируется не только твердыми телами, но и жидкостями, в которых он мало растворим. Однако некоторые соли образуют с ним комплексы, что используют для сорбции оксида углерода водно-аммиачными растворами солей одновалентной смеси.
Водород – второй компонент синтез – газа – наиболее трудно сжижаемый газ (температура конденсации при атмосферном давлении – 252,80С). Образует с воздухом взрывоопасные смеси в пределах 4,0 – 75 % (об.) Н2. Наряду с высокой взрывоопасностью оксида углерода это предъявляет повышенные требования к технике безопасности при производстве синтез-газа, а также в цехах, где он служит сырьем для органического синтеза.
Для производства синтез-газа вначале использовали уголь. Затем преобладающее значение получила конверсия углеводородов, которую осуществляют в двух вариантах: каталитическом и высокотемпературном. Сырьем для нее может служить метан или природный газ, а также жидкие фракции нефти.
При сгорании предельных углеводородов выделяется большое количество тепла, поэтому природный газ является самым эффективным и дешевым топливом для теплоэлектростанций, котельных установок, доменных и стекловаренных печей. Кроме того, при сгорании метана воздух практически не загрязняется вредными веществами.
Метан природного и попутного нефтяного газов является важным сырьем для химической промышленности. Конверсией метана получают синтез-газ, а на его основе – метанол и синтетический бензин:
Гомологи метана, содержащиеся в природном и, главным образом, в попутном нефтяном газах, после разделения на индивидуальные углеводороды идут на получение алкенов и далее полимеров. Пропан-бутановая фракция в сжиженном виде используется как бытовое топливо и топливо для карбюраторных двигателей автомобилей. Газовый бензин, получаемый из попутного газа, также является основой низкосортных бензинов.
Основная реакция, лежащая в основе этого метода, состоит в конверсии углеводородов водяным паром на катализаторе Ni на AI2O3:
Реакция сильно эндотермична, и ее равновесие смещается вправо лишь при повышении температуры. Чтобы увеличить степень конверсии метана, ведут процесс при 800 – 900°С в избытке водяного пара. При атмосферном давлении этот избыток невелик (2:1), но повышение давления неблагоприятно влияет на состояние равновесия, и в этом случае приходится работать с объемным отношением пара к метану ≈ 4:1.
Кроме конверсии метана протекает также конверсия оксида углерода:
Эта реакция экзотермична, и ее равновесие при повышении температуры смещается влево, причем избыток водяного пара вызывает повышенное образование диоксида углерода. Конверсия оксида углерода протекает быстро, и состав конвертированного газа определяется ее равновесием.
При конверсии метана водяным паром получается газ с большим отношением Н2:СО (как минимум 3:1), в то время как для органического синтеза требуется синтез-газ с отношением Н2:СО от 1:1 до (2 ÷ 2,3):1. Этого отношения можно добиться, подвергая конверсии жидкие углеводороды:
И добавляя при конверсии к водяному пару диоксид углерода, который также конвертирует углеводороды:
Реакция эндотермична, и ее равновесие смещается вправо при достаточно высокой температуре. Она протекает медленнее, чем конверсия водяным паром.
Ввиду высокой эндотермичности конверсию углеводородов проводят в трубчатых печах (рис. 1). Исходное сырье подают в трубы, заполненные гетерогенным катализатором и обогреваемые топочным газом, причем теплопередача осуществляется главным образом за счет излучения (радиантные печи). Недостатки этой системы – большая потребность в жаростойких трубах и малое полезное использование объема печи, в которой катализатор занимает очень небольшую часть.
По этим причинам была разработана другая система, в которой эндотермические реакции конверсии совмещены с экзотермическим процессом сгорания части углеводорода при подаче в конвертор кислорода, благодаря чему суммарный процесс становится немного экзотермическим. Расчеты показывают, что для этой цели на конверсию надо подавать смесь СН4 и О2 в отношении 1 : 0,55, находящуюся вне пределов взрываемости, которые тем более не достигаются из-за разбавления смеси водяным паром. Объемное отношение последнего к метану в этом случае можно брать более низким, чем в отсутствии кислорода, а именно от 1:1 до (2,5÷3):1 в зависимости от применяемого давления. Этот процесс окислительной, или автотермической конверсии получил большое распространение. Он не требует подвода тепла извне и осуществляется в шахтных печах со сплошным слоем катализатора (рис. 2).
Корпус конвертора футерован огнеупорным кирпичом и имеет охлаждающую водяную рубашку, в которой генерируется пар. В верхней части конвертора имеется смеситель, куда подают смеси СН4 + Н2О и О2 + Н2О. Смеситель должен обеспечить гомогенизацию смеси в условиях, исключающих взрыв или воспламенение. Сгорание метана протекает примерно в 10 раз быстрее конверсии, поэтому в верхних слоях катализатора температура быстро повышается до максимума (1100 – 12000С) и затем падает (до 800 – 9000С) на выходе из печи. По сравнению с конверсией в трубчатых печах при этом методе устраняется потребность в жаростойких трубах, конструкция реактора становится очень простой и большая часть его объема полезно используется для размещения катализатора. При окислительной конверсии в получаемом газе несколько возрастает количество СО.
Процесс состоит из нескольких стадий: подготовки сырья, конверсии, утилизации тепла, очистки газа от СО2. При подготовке сырья следует иметь в виду, что никелевый катализатор чувствителен к отравлению органическими соединениями серы, содержание которых в углеводороде ограничивают величиной 1 мг S в 1 м3. Сырье, не удовлетворяющее этим условиям, нужно очищать, для чего подвергают каталитическому гидрообессериванию с последующим удалением образовавшегося сероводорода. Стадия подготовки сырья включает также компримирование газа, смешение его с водяным паром и предварительное нагревание смеси.
Принципиальная схема окислительной конверсии метана (или природного газа) при высоком давлении приведена на рис. 3.
Исходный метан, очищенный от сернистых примесей, сжимают турбокомпрессором 1 до 2 – 3 МПа и смешивают с необходимым количеством водяного пара и СО2. Смесь подогревают в теплообменнике 2 до 4000С частично охлажденным конвертированным газом и подают в смеситель конвертора 6, куда поступает предварительно приготовленная смесь кислорода с равным объемом водяного пара. Конвертор охлаждается кипящим в рубашке конденсатом; при этом генерируется пар давлением 2 – 3 МПа, который отделяют в паросборнике 5. Тепло горячего конвертированного газа, выходящего из конвертора при 800 – 9000С, используют в котле-утилизаторе 4 для получения пара высокого давления, направляемого затем в линию пара соответствующего давления или используемого для привода турбокомпрессора. Тепло частично охлажденного газа утилизируют для предварительного подогревания смеси в теплообменнике 2 и в теплообменнике 3 для нагревания водного конденсата, питающего котел-утилизатор. Окончательное охлаждение газа осуществляют в скруббере 7 водой, циркулирующей через холодильник 8.
Полученный на этой стадии синтез-газ в зависимости от требований к соотношению СО и Н2 содержит 15 – 45 % (об.) СО, 40 – 75 % (об.) Н2, 8 – 15 % (об.) СО2, 0,5 % (об.) СН4 и по 0,5 – 1 % (об.) N2 и Ar. Этот газ очищают от СО2, для чего применяют абсорбцию водой под давлением, хемосорбцию водным раствором моноэтаноламина или карбоната калия. При нагревании и снижении давления происходят обратные превращения и выделяется СО2, а раствор регенерируется:
Http://pandia. ru/text/77/504/4381.php
Большие масштабы потребления водорода и его смесей с азотом, окисью и двуокисью углерода требуют постоянного совершенствования технологии их получения, оптимизации и интенсификации крупнотоннажных промышленных процессов каталитической конверсии природного газа. Природный газ, содержащий от 90 до 99% об. метана, в последнее время стал основным сырьем для производства водорода. Роль процессов газификации твердых топлив, занимавших в прошлом доминирующих положение в мировом производстве водорода, в наши дни продолжает непрерывно понижаться. Достаточно широко перерабатываются также жидкие углеводороды нефти и газообразные гомологи метана, удельный вес которых в сырьевой базе производства заметно увеличился. Водород может использоваться в народном хозяйстве как и в чистом виде (процессы гидроочистки и гидрокрекинга в нефтепереработке), так и в виде смесей с азотом или двуокисью углерода (в производствах аммиака, спиртов, моторных топлив).
В связи с этими направлениями процессы каталитической конверсии метана можно разделить на следующие основные способы:
Процессы каталитической конверсии природного газа по (1) и (2) способам с последующей конверсией окиси и очистки от двуокиси углерода предназначены для получения чистого водорода. Процессы парокислородовоздушной конверсии с последующей конверсией окиси углерода, отчисткой от двуокиси углерода и тонкой доочисткой от следов окиси углерода предназначены для получения азотоводородной смеси. Процессы пароуглекислотной конверсии осуществляются с целью получения смеси, состоящей из водорода и окиси углерода в различных соотношениях, направляемую для синтеза спиртов различного молекулярного веса.
Поскольку в процессах паровой и пароуглекислотной конверсии метана протекают эндотермические реакции, то для поддержания необходимой температуры в зоне реакции избыточное количество тепла подводится извне путем обогрева реакционных труб печи, заполненных катализатором, горячими топочными газами.
При автотермической конверсии тепло, необходимое для проведения процесса, выделяется непосредственно в реакционной зоне в результате сгорания в потоке кислорода части исходного углеводородного сырья и продуктов конверсии-окиси углерода, и водорода. В процессах комбинированной конверсии на первой ступени конвертируется определенная часть метана с водяным паром в трубчатой печи, затем конвертированный газ поступает в шахтный реактор, где в присутствии воздуха производится полная конверсия метана.
Производства-потребители в зависимости от их технологии предъявляют неодинаковые требования к составу и чистоте водорода и синтез-газа. Так, каталитические процессы производства аммиака требуют тщательной очистки азотоводородной смеси от окиси и двуокиси углерода, а в процессах синтеза спиртов и оксосинтеза окись углерода является стехиометрически необходимым компонентом. Водород в процессах гидроочистки нефтяных дистиллятов также не требует тонкой очистки от примесей окиси и двуокиси углерода.
В качестве катализаторов в процессах конверсии метана обычно используют никель, нанесенный на различные термостойкие носители(шамот, окись алюминия, цеолиты, соединения бора, корунд, графит, хром, магний и др.).
С целью обеспечения прочности катализаторов при прессовании в его состав на последнем этапе приготовления добавляют 2-3 вес. части графита. Для прочности контакта в состав добавляют бор, а для обеспечения пористости в состав добавляют летучие вещества, которые при нагревании улетучиваются и создают необходимую пористость.
Как известно, никель относится к классу окислительно-восстановительных катализаторов. Никелевые катализаторы широко применяются и в процессах гидрирования и дегидрирования углеводородов.
На технико-экономические показатели процесса существенное влияние оказывают соединения серы в исходном природном газе, которые являются ядом для никелевых катализаторов. В связи с этим требуется дополнительная установка сероочистки исходного газа.
Проведение технологических процессов конверсии при недостатке окислителей приводит к выпадению свободного углерода, который покрывает поверхность катализатора и снижает его механическую прочность. Термодинамический анализ равновесия реакций конверсии показывает, что вероятность выделения элементарного углерода или так называемая область зауглероживания, определяется содержанием углеводорода в исходной конвертируемой смеси. Количество выделяющегося углерода увеличивается с повышением парциального давления углеводорода и с увеличением соотношения С : Н в нем. При проведении процесса конверсии с избыточным по сравнению со стехиометрически необходимым количеством окислителей удается предотвратить образование элементарного углерода. Однако это не свидетельствует о том, что реакция образования углерода является побочной, сопутствующей основным реакциям конверсии углеводородов.
Анализ большого экспериментального материала по механизму реакций, протекающих в процессах конверсии метана показывает, что каталитическая конверсия протекает многостадийно через окисление-восстановление катализатора и образование газификации углерода на катализаторе.
Следовательно, стадию углеобразования следует рассматривать как составную часть суммарного процесса каталитической конверсии. Об этом свидетельствует экспериментально установленные факты сохранения и даже возрастания активности катализатора при наличии углерода.
Наиболее существенным параметром, позволяющим устранить опасность образования элементарного углерода в процессах конверсии, являет соотношение окислитель : углеводород. Как это видно из стехиометрии реакций
Соотношение окислитель : углеводород пропорционально числу углеродных атомов углеводорода.
Это означает, что процесс конверсии высокомолекулярных гомологов метана и жидких углеводородов будет протекать при большем расходе окислителей по сравнению с конверсией метана. Как правило, паровую конверсию метана проводят с двукратным избытком водяного пара по сравнению со стехиометрическим, а парокислородную – при соотношении водяной пар: метан равным единице и расходе кислорода на процесс 0,55-0,65 мол/моль метана. Из (1.1) и (1.2) следует, что кислород как окислитель эквивалентен двум молям водяного пара. Следовательно, в пересчёте на водяной пар соотношение окислитель : метан в процессах парокислородовоздушной конверсии составит 1,1-2,3 моль/моль. Т. е. по этому показателю оба способа конверсии близки. Промышленные процессы конверсии метана осуществляются при атмосферном и повышенном давлениях. В первом случав процесс протекает в сравнительно простой и дешевой аппаратуре при высокой степени превращения исходного сырья. Повышение давления термодинамически не благоприятствует процессу конверсии. Однако, в ряде случаев экономичнее проводить процесс при повышенном давлении (17-70 ата).
Применение давления имеет определенные преимущества в тех случаях, когда получаемый водород или синтез-газ используют для синтезов под’ давлением. При этом снижаются затраты на компремирование газа в процессе его дальнейшей переработки. При повышенном давлении, кроме того уменьшается объём аппаратов и трубопроводов.
Как было выше сказано, что производства, потребляющие водород или его смеси, предъявляют жесткие требования к составу синтез-газа. Та, для аммиачных производств требуется синтез-газ с содержанием остаточного метана не более 0,5% об. Расчеты показывают, что для получения синтез-газа с содержанием метана меньше 0,6% об., реакционные аппараты промышленных агрегатов конверсии природного газа должны обеспечить при принятых режимах, близкую к равноценном степень прекращения мотана. Эта особенность позволяет определить материальный баланс, технико-экономические показатели, решать, некоторые задачи оптимизации и интенсификации процессов конверсии по термодинамическим равновесиям реакций. Поэтому вполне понятно, что расчетам равновесия реакции, протекающих в процессах конверсии углеводородов (преимущественно метана) водяным паром, углекислотой, кислородом и их смесями, посвящено достаточно много работ. Следует отметить, что проектирование промышленных процессов конверсии метана осуществлялось до сих пор также путем термодинамических расчетов. Этим, по видимому, и обуславливалось, недостаточное внимание исследователей вопросам механизма и кинетики процессов конверсии, подбору и разработке оптимальных катализаторов и оптимальному проектированию реакционных аппаратов.
Http://studfiles. net/preview/576446/
КАТАЛИТИЧЕСКИЕ МЕТОДЫ ПОДГОТОВКИ И ПЕРЕРАБОТКИ ПОПУТНЫХ НЕФТЯНЫХ ГАЗОВ
Как уже было упомянуто ранее, одной из основных задач является очистка ПНГ от сероводорода. Для решения этой задачи предлагается технология селективного окисления сероводорода до серы: H2S + О2 > S + Н2О. Основными преимуществами процесса являются его непрерывность, мягкие условия его осуществления при температурах 200—250°С, когда превращения других компонентов ПНГ не происходит. Этому способствует применение специальных оксидных катализаторов. В зависимости от содержания сероводорода в очищаемых газах используются два варианта технологического оформления процесса. При высоком содержании сероводорода в ПНГ (15—80% об.) применяются каталитические реакторы с псевдоожиженным слоем катализатора (см. рис. 1А). Если концентрация H2S менее 10—15% об., то используют каталитические реакторы с блочным сотовым катализатором (см. рис. 1Б). Данная технология разработана под руководством проф. З. Р. Исмагилова и защищена патентами в России, США, Канаде, Франции и других странах.
Перед транспортировкой ПНГ требуется провести его глубокую осушку от паров воды. Для этого предлагается использовать разработанные в Институте катализа СО РАН под руководством доктора химических наук Ю. И. Аристова композиционные нано-пористые адсорбенты. При пропускании ПНГ с парами воды через зернистый слой нанопористого материала, например, оксида алюминия, содержащего внутри пор безводную соль (СаС L2 ) будет происходить активное поглощение влаги и ее связывание в виде твердых кристаллогидратов типа СаС1 2 n Н 2 0 внутри пор. Емкость композиционных материалов типа "соль в нанопористой матрице" очень велика и достигает 0,6—1,0 г H 2 О/г материала. Материал после поглощения даже такого количества влаги остается сыпучим. Для восстановления сорбционных свойств материала его нагревают до температур 100-130°С, при которых происходит разложение кристаллогидратов и композиционный материал-сорбент оказывается готовым к повторному использованию.
Следует обратить внимание на то, что целевое протекание реакций (т. е. слева направо) возможно только при Т>Т*.
Селективность превращения пропан-бутановой фракции в ароматические углеводороды достигает 70—72%, а выход арома-тики достигает 40% за проход.
□ Состав природного газа: метан 80 % об, этан 4 % об., пропан/бутан 2 % об.
Особый интерес представляет разработка областей применения таких наноуглеродных материалов. Прежде всего следует обратить внимание на области крупнотоннажного использования таких материалов — это дорожные и строительные материалы. Введение наноуглеродных материалов в количестве менее 1% масс в бетоны повышает их прочность на 40—50%. Это, соответственно, будет облегчать вес строительных конструкций и снижать себестоимость строительства. Перспективным является применение таких углеродных материалов в производстве композиционных полимеров. Это придает полимерам новые свойства — электропроводность, морозостойкость и механическую прочность.
Http://sinref. ru/000_uchebniki/0000AZS/024_inovac_tehnologii_poput_gaz_2010/020.htm
Конверсия природного газа в настоящее время является основным методом получения водорода и синтез-газа (смеси Н2 и СО). В зависимости от используемого окислителя и аппаратурного оформления различают высокотемпературную кислородную конверсию, каталитическую парокислородную конверсию в шахтных печах и каталитическую пароуглекислотную конверсию в трубчатых печах. Окисление метана протекает по следующим основным интегральным реакциям:
В зависимости от последующего применения принципиальные схемы конверсии природного газа могут различаться. Независимо от этого на первом этапе природный газ подвергают компремированию до 2-4 МПа и направляют в отделение сероочистки, Природный газ содержит существенное количество серусодержащих соединений, среди которых можно выделить Н2S, CS2, COS, CH3SH, C2H5SH и другие. Для достижения допустимого уровня содержания соединений серы (1мг/м 3 ) применяют двухступенчатую очистку.
На первой стадии сераорганические соединения гидрируют с использованием алюмокобальтмолибденового или алюмоникельмолибденового катализатора при температуре 350-400°С и давлении 2-4МПа. Реакции гидрирования при указанных условиях практически необратимы, в результате образуются предельные и непредельные углеводороды, монооксид углерода и сероводород. На второй ступени очистку от сероводорода производят поглотителем на основе оксида цинка (ГИАП-10) при температуре 390-410°С.
Равновесный состав конвертированного газа зависит также от температуры и давления исходной смеси. Конверсия углеводородов идет с увеличением объема и с поглощением теплоты. Согласно принципу Ле-Шателье, химическое равновесие реакций (8.1.1.-8.13) смещается в сторону образования продуктов при повышении температуры и уменьшении давления.
Однако проведение каталитической конверсии метана под давлением 2-3 МПа значительно экономичнее, так как промышленный синтез аммиака и метанола, а также ряда других продуктов, в которых используют водород, смесь водорода с азотом или монооксидом углерода, осуществляется при высоком давлении. В этом случае резко снижается расход энергии на сжатие конвертированного газа, из-за возможности использования естественного давления транспортируемого природного газа, улучшаются технико-экономические показатели производства аммиака и метанола, уменьшаются капитальные затраты на строительство установок. Кроме того, повышение давления приводит к уменьшению объемов газа и, соответственно аппаратуры и газопроводов, что позволяет создавать агрегаты большой мощности при сравнительно небольших габаритах аппаратуры.
С повышением температуры степень превращения метана возрастает. Так при давлении 1 ат, отношении CH4 : H2O=1 : 2 и температурах 527, 627, 727 и 827 о С степень превращения СН4 в случае равновесия достигает соответственно 40,9; 73,4; 95,8 и 99,6
Согласно расчетам, практически полное превращение метана происходит при 800 о С, если объемное соотношение пар : газ составляет не менее 2 : 1. Однако в отсутствии катализатора скорость реакции взаимодействия метана с водяным паром очень мала и поэтому термодинамическое равновесие в области температур 700-1050 о С не достигается.
Для достижения при температуре 800-830 о С практически полного превращения метана (остаточное содержание метана около 1 %(об.)) отношение СН4:Н2О в исходной смеси должно составлять приблизительно 1 : 2 при давлении близком к атмосферному; 1 : 4 при давлении 10 ат, 1 : 6 при 20 ат и 1 : 8 при 30 ат.
Конверсию природного газа водяным паром проводят при давлении 2МПа и соотношении исходных реагентов СН4:Н2О=1:4. В этом случае остаточное содержание метана составляет 8-10%( объёмных). Для достижения остаточного содержания метана на уровне 0,5%(объёмных), конверсию ведут в две стадии: паровоздушная конверсия под давлением и паровоздушная конверсия с использованием кислорода воздуха. В качестве катализаторов конверсии природного газа используют никелевые катализаторы на оксиде алюминия, выпускаемые промышленностью в виде таблетированных или экструдированных колец Рашига. Эти катализаторы должны быть высокоактивными, стабильными, термостойкими и механически прочными. Срок службы лучших современных никелевых катализаторов составляет не менее 3 лет.
Применяются два основных способа приготовления катализаторов. По первому, соединения никеля и промоторов смешивают с порошкообразным носителем. Для смешивания окислов нескольких металлов используют соосаждение их в виде гидратов, окислов, карбонатов. Образующаяся при этом однородная масса формируется либо в мокром виде – экструзией, либо в полусухом и сухом состоянии – таблетированием. Катализаторы выпускают, в основном, в форме цилиндрические таблеток или колец диаметром и высотой 8-20 мм. По второму способу каталитические веществ наносят на сформованный и прокаленный инертный носитель путем пропитывания его раствором солей никеля и промоторов. Готовый катализатор, независимо от способа приготовления, прокаливают при 400-450 о С для перевода солей никеля и промоторов в форму оксидов и для спекания порошка. Восстановление катализаторов проводят непосредственно в реакционном аппарате. Содержание никеля в различных катализаторах составляет 4-30 масс.%
Срок службы катализаторов конверсии природного газа при правильной эксплуатации достигает трёх и более лет. Никелевые катализаторы наиболее чувствительны к воздействию сернистых соединений вследствие образования на поверхности катализатора неактивного сульфида никеля. Отравленный соединениями никеля и углеродом катализатор может быть регенерирован при подаче очищенного от соединений серы природного газа и значительного количества водяного пара.
В случае необходимости получения чистого водорода, а не синтез-газа проводят процесс каталитической конверсии монооксида углерода, которая протекает по реакции (8.1.4). В соответствии с условиями термодинамического равновесия повышение степени конверсии Со может быть достигнуто при удалении диоксида углерода из газовой смеси, увеличении содержания водяного пара и уменьшении температуры. Повышение давления не смещает равновесие, так как реакция идёт без изменения числа молей, но увеличивает скорость реакции, что приводит к уменьшению габаритов оборудования, полезно используется энергия ранее сжатого газа. Мольная доля водяного пара в исходной газовой смеси определяется количеством, подаваемым на конверсию природного газа, в результате соотношение Н2О:СО составляет порядка 2:1. Реакция конверсии СО сопровождается значительным выделением теплоты, что определяет двухстадийную организацию процесса. Температурный режим каждой стадии определяется свойствами применяемых катализаторов. На первой стадии используется среднетемпературный железохромовый катализатор. Низкотемпературные катализаторы содержат в своём составе соединения меди, цинка, алюминия и ряд других элементов, которые повышают термостабильность катализатора. Перед началом работы низкотемпературный катализатор восстанавливают водородом или СО. Срок службы низкотемпературных катализаторов обычно не превышает двух лет.
Агрегат двухступенчатой конверсии природного газа и монооксида углерода работает следующим образом. Природный газ сжимают в компрессоре до давления 4, МПа, смешивают с азотоводородной смесью в соотношении 10:1 подают в огневой подогреватель, где реакционная смесь нагревается до температуры 370-400 о С. Далее последовательно производится гидрирование сернистых соединений в каталитическом реакторе на алюмокобальтмолибденовом катализаторе и адсорбере, где сероводород поглощается оксидом цинка. Очищенный газ смешивается с водяным паром в соотношении 1:3,7 и направляется в конвекционную зону трубчатой печи. В радиационной камере размещены трубы, где расположен катализатор конверсии метана и горелки, в которых сжигается природный газ. Парогазовая смесь нагревается до температуры 525 о С и под давлением 3,7 МПа распределяется по больщому количеству параллельно включённых труб. Выходящая парогазовая смесь содержит 9-10 % (объёмных) СН4. При температуре 850 о С конвертированный газ поступает в шахтный реактор, в верхнюю часть которого подаётся технологический воздух при температуре 480-500 о С. По окончании конверсии газ с температурой 1000 о С и остаточным содержанием метана 0,5 % (объёмных) направляется в котёл-утилизатор и при температуре 450 о С направляется на двухступенчатую конверсию монооксида углерода. Схемы аппаратурного оформления процесса конверсии можно найти в учебниках ОХТ, приведённых в списке литературы.
Аммиак широко используется в производстве удобрений (аммиачной селитры – NH4NO3; карбамида – (NH2)2CO; сульфата аммония; аммофоса-NH4H2PO4; нитрофоса-смесь CaHPO4∙2H2O, NH4NO3 и гипса; нитрофоски – смесь CaHPO4∙2H2O, аммофоса и NH4NO3), полимерных материалов (полиамидов – найлона, капрона; полиакрилнитрила; полиуретанов), взрывчатых веществ (тротила, аммонита), фотографических препаратов, медикаментов и ряда других важных продуктов.
Реакция обратимая, экзотермическая, характеризующаяся большим отрицательным энтальпийным эффектом (DH298=-91,96 кдж/моль NH3) и протекающая с уменьшением числа молей. Поэтому, согласно принципа Ле Шателье, нагревание равновесной смеси смещает равновесие в сторону образования азота и водорода; повышение давления – в сторону образования аммиака (табл. 8.2.1). Следовательно, с точки зрения условий термодинамического равновесия максимального выхода аммиака можно достичь, проводя процесс синтеза при высоких давлениях и низких температурах. Однако, с позиций кинетики химических реакций, для увеличения скорости синтеза аммиака процесс надо проводить при высоких температурах.
Http://megaobuchalka. ru/5/3144.html
Так как на современном нефтеперерабатывающем заводе имеется большое число установок гидрокрекинга и гидроочистки, то важное значение приобретает обеспечение их водородом.
Источником водорода на нефтеперерабатывающем заводе обычно является установка каталитического риформинга. Легкокипящая фракция, поступающая с этой установки, характеризуется высоким соотношением водород/метан; обычно ее подвергают деэтанизации и депропанизации, чтобы повысить концентрацию водорода.
Иногда водорода с установки риформинга оказывается недостаточно, чтобы удовлетворить все потребности нефтеперерабатывающего завода, например, если работает установка гидрокрекинга. Тогда водород получают на установке конверсии метана с водяным паром, которая показана на рисунке ниже. 1) Метан используется по той причине, что в его молекуле содержится 25 % (масс.) водорода. 2)
При поиске возможностей синтеза водорода в качестве потенциального сырья рассматривались различные соединения с высоким содержанием водорода, чтобы получалось как можно меньше отходов и как можно меньше энергии было потрачено впустую. Два соединения, которые в конце концов выбрали, кажутся достаточно очевидными — это метан (СН4) и вода (Н2О).
Задача процесса конверсии метана с водяным паром состоит в том, чтобы извлечь из этих соединений как можно больше водорода, затратив при этом как можно меньше энергии (топлива). Этот процесс осуществляется в четыре стадии с помощью некоторых полезных катализаторов.
1. Конверсия. Метан и водяной пар (Н2О) смешивают и пропускают над катализатором при 800°С (1500°F), в результате чего образуется монооксид углерода и водород.
Без катализатора паровая конверсия метана с приемлемой скоростью и глубиной превращения протекает при 1250…1350 °С. Катализаторы конверсии углеводородов предназначены не только для ускорения основной реакции, но и для подавления побочных реакций пиролиза путем снижения температуры конверсии до 800…900 °С. Как наиболее активные и эффективные катализаторы конверсии метана признаны никелевые, нанесенные на термостойкие и механически прочные носители с развитой поверхностью типа оксида алюминия. С целью интенсификации реакций газификации углерода в никелевые катализаторы в небольших количествах обычно вводят щелочные добавки (оксиды Са и Mg). 4)
2. Дополнительная конверсия. Не удовлетворившись водородом, который уже образовался, установка выжимает все, что можно, и из монооксида углерода. К смеси прибавляют дополнительное количество водяного пара и пропускают над другим катализатором при 340°С (650°F); в результате образуется диоксид углерода и водород.
3. Разделение газов. Чтобы получить поток с высоким содержанием водорода, его отделяют от диоксида углерода с помощью процесса экстракции диэтаноламином (ДЭА).
4. Метанирование. Поскольку присутствие даже небольших количеств оксидов углерода в потоке водорода может оказаться вредным для некоторых областей его использования, на следующей стадии процесса эти примеси превращаются в метан. Процесс идет на катализаторе при 420°С (800°F).
Подробная технологическая схема установки для получения водорода паровой каталитической конверсией представлена на следующем рисунке. На ней вы можете увидеть, в каком оборудовании протекают четыре описанные выше стадии.
Газ под давлением подогревают до 300—400°C в подогревателе 7 и подают в реакторы 3 и 2, где он очищается от сернистых соединений. В смесителе 11 смешивают газ с перегретым до 400—500°C водяным паром и подают паро-газовую смесь на конверсию в печь 12. Температура конверсии 800—900°C.
Газ конверсии из общего коллектора проходит котел-утилизатор 13, где охлаждается до 400—450°C (эту температуру поддерживают, впрыскивая воду после котла-утилизатора). Для превращения CO в CO2 газ подают на первую ступень среднетемпературной конверсии в реактор 14 с железо-хромовым катализатором; после этого температуру паро-газовой смеси снова снижают до 230-250°C в котле-утилизаторе 13 и в водоподогревателе 15; смесь направляют на вторую ступень конверсии в реактор 16 с цинк-медным катализатором.
Затем паро-газовая смесь, содержащая водород, диоксид углерода и водяные пары, поступает на очистку от CO2 в абсорбер 18. В результате очистки раствором карбоната калия (K2CO3) удаляют CO2 и большую часть водяных паров. Раствор K2CO3 идет на регенерацию, а водород подогревают до 300°C в теплообменнике 25 и подают в реактор 22 на метанирование, т. е. переводят оставшийся CO в метан путем гидрирования. Затем водород охлаждают в теплообменнике 25 и холодильнике 23. Компрессор 24 сжимает водород до требуемого давления на выводе с установки к месту потребления. 6)
В некоторых случаях в распоряжении переработчиков не оказывается метана, не содержащего серы (природного газа). В этом случае вместо метана можно использовать более тяжелые углеводороды, например пропан или нафту. Такой процесс требует другого оборудования и других катализаторов. Кроме того, он менее энергетически эффективен, но все же работает.
Установка производства водорода методом паровой конверсии легких углеводородов
Http://wiki. unitechbase. com/doku. php/courses:refining:%D0%BF%D1%80%D0%BE%D0%B8%D0%B7%D0%B2%D0%BE%D0%B4%D1%81%D1%82%D0%B2%D0%BE_%D0%B2%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B4%D0%B0